生物制剂已经成为许多炎性风湿病治疗策略的核心组成部分。然而,由于生物制剂的特异性和普遍的高亲和力,风湿病学家广泛使用生物制剂疗法时与使用常规合成DMARDs药物时相比,较少考虑药代动力学的情况。通常认为免疫原性是在生物制剂早期研发阶段限制其使用的重要因素,然而法规指导相对有限,并且测量免疫原性的测定方法也不如今天复杂。生物仿制药的出现激发了人们对免疫原性的新兴趣,从而引起了越来越敏感的检测方法的发展,人们对免疫原性的药代动力学结果的认识增强,监管机构制定了全面而具体的指南。因此,风湿病学家对该领域的总体了解大大提高,包括造成免疫原性的因素,其潜在的临床后果以及对日常治疗的影响。在某些专业中,免疫原性测试已成为常规临床管理的一部分,但它在风湿病学中的成本效益的确切证据还有待证实。
2020年12月,发表于风湿领域权威杂志《Nature Reviews Rheumatology》(影响因子IF:16.625)的一篇综述详述了风湿病学中生物制剂的免疫原性。

关键点
1.所有生物制剂都具有免疫原性,许多途径影响其生物利用度,包括患者特异性因素、疾病特异性特征和遗传背景。
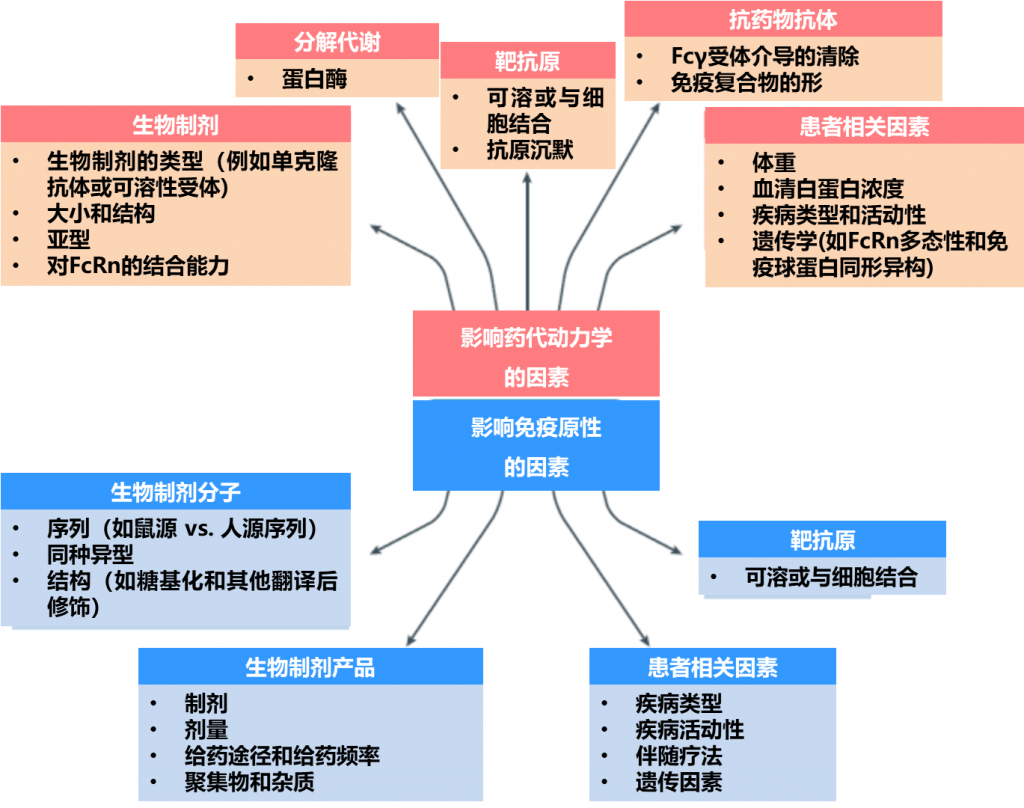
影响生物制剂的药代动力学和免疫原性的因素如下图所示:
各种因素均可影响生物制剂的药代动力学,包括与药物本身有关的因素(生物制剂的类型、大小和结构,最初Fc受体(FcRn)的亚型或结合亲和力),目的抗原(抗原是细胞结合的还是可溶的,以及其表达水平),可消化药物的蛋白酶的存在,抗药物抗体的发展(包括免疫复合物的形成和通过Fcγ受体(FcγR)结合加速清除)和患者相关因素(所治疗的疾病和疾病活动性、患者体重、血清白蛋白浓度和遗传因素)。许多因素也会影响生物制剂的免疫原性,包括与药物本身有关的因素(主要序列,同种异型和翻译后修饰,例如糖基化),靶抗原(可溶或与细胞结合), 最终药品(制剂、给药方案、给药途径、存在杂质或聚集体)和患者相关因素(所治疗的疾病,疾病活动性,伴随疗法、例如同时服用甲氨蝶呤,遗传因素)。
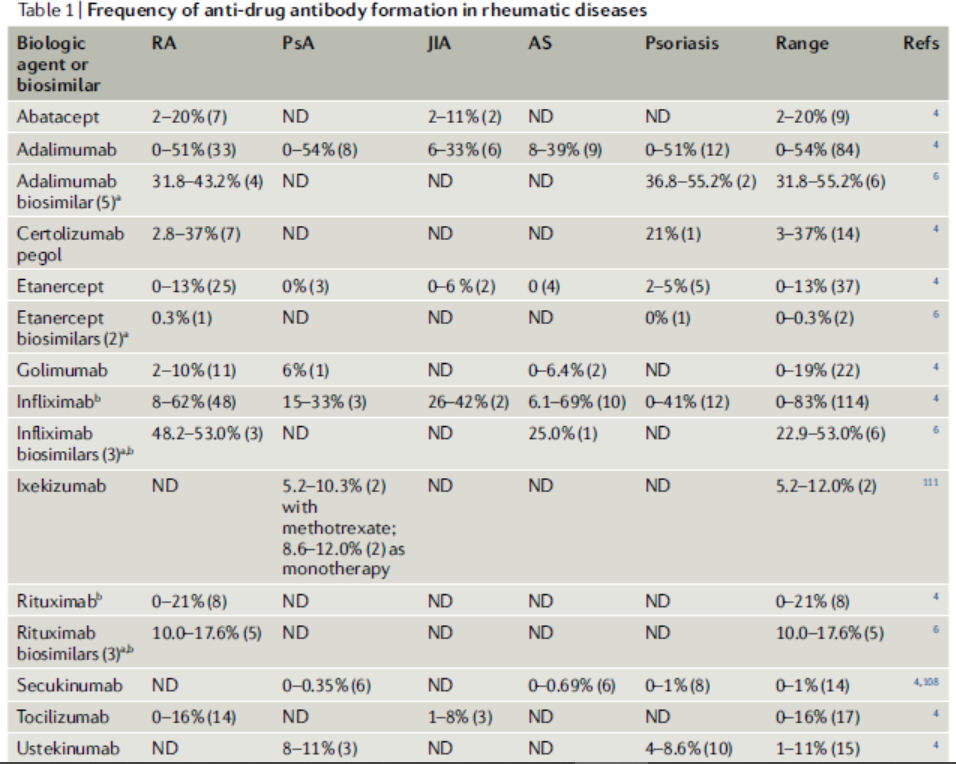
理论上,人源化抗体应该比嵌合抗体具有更低的免疫原性,因为在可变区存在较少的非人类蛋白序列,这些序列可能被认为是外来的。如英夫利昔单抗(五种可用的TNF抑制剂中唯一的嵌合单克隆抗体)比其他四种TNF抑制剂更具有免疫原性。关于嵌合抗体、人源化抗体和完全人源化抗体的免疫原性的争论已经持续了很长时间,从本文综述的数据表明,全人源抗体可能是免疫原性最低的。见下表:
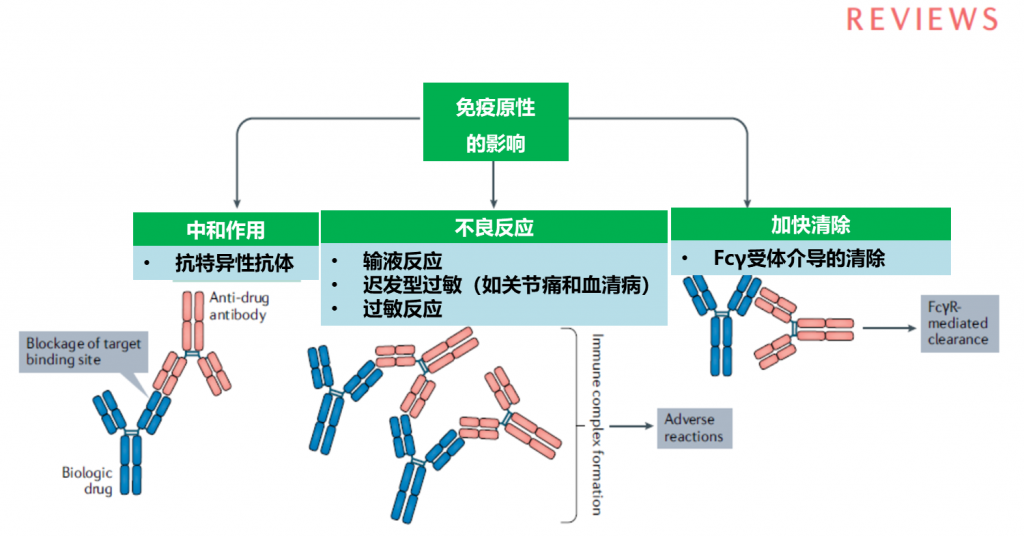
2.免疫原性的潜在影响范围从无临床影响到治疗效果降低、输液反应,以及罕见的血清病或过敏反应。
4.现有免疫原性试验之间最重要的区别是该试验的耐药程度。
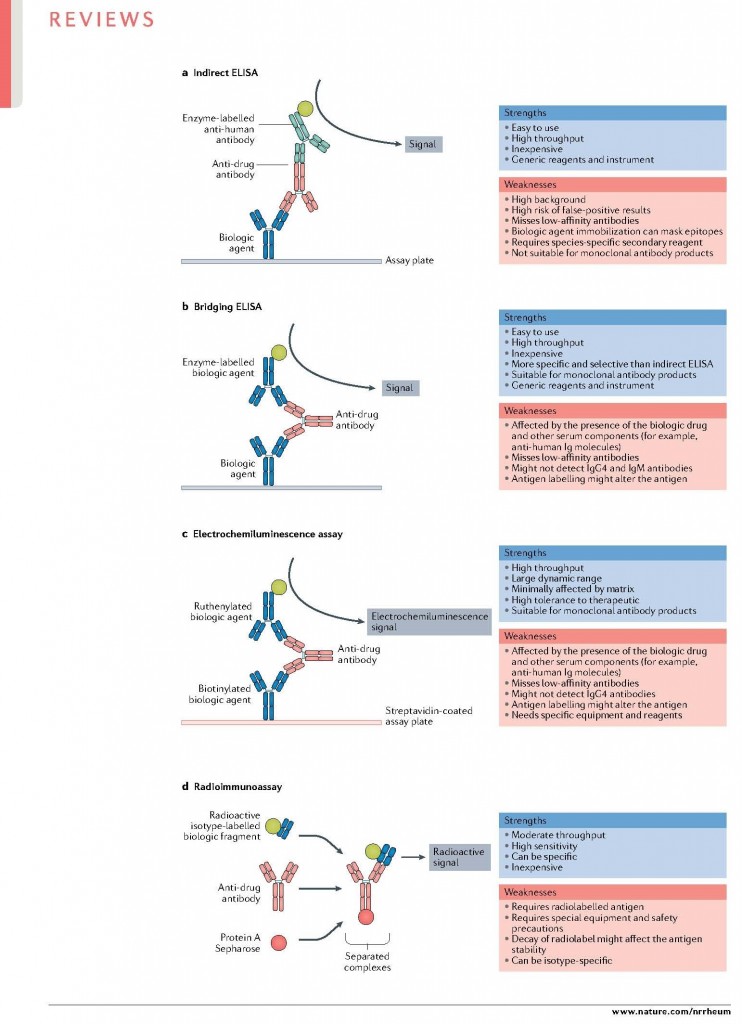
ADAs的检测和评价是一个复杂的过程,其结果可能会受到所使用的分析方法的影响。因此,在评估免疫反应时,使用特定的和批准的策略是重要的。筛选试验必须敏感、特异,并能够识别给定生物制剂的所有ADAs亚型。评估免疫原性的方式包括不同类型的免疫分析,如酶联免疫吸附分析(ELISAs)、电化学发光免疫分析(ECLIAs)和放射免疫分析,以及不同的免疫分析形式,如直接、间接、桥接和竞争等形式。下图显示了常用的抗药物抗体(ADA)检测免疫分析形式及其优缺点。
图a对于间接酶联免疫吸附试验(ELISAs),生物制剂涂布在测定板上,以捕获样品中存在的任何ADAs;然后这些抗体被偶联酶的抗人IgG抗体检测,该酶能提供比色或化学发光信号。
图b桥接ELISAs是将生物制剂直接涂布到测定板上。根据可选的酸解预处理步骤加入患者样本,并通过平板结合药物捕获任何存在的ADAs。然后使用酶标记的生物制剂检测捕获的ADAs,因此任何存在的ADAs必须与两种生物制剂(平板结合剂和标记生物制剂)结合才能发出信号。其它用于检测ADAs的ELISA方法使用抗人λ链结合抗体作为检测抗体,而不是标记生物制剂。
图c在电化学发光免疫分析法中,在酸解预处理步骤之后,样品与钌化和生物素化形式的生物制剂孵育,该生物制剂与任何存在的ADAs结合。然后将样本加到链霉亲和素涂布的平板上,捕捉ADAs生物制剂复合物。在三丙胺存在和施加电流的情况下,钌产生化学发光信号。
图d在放射免疫检测中,蛋白A琼脂糖凝胶捕获血清ADAs,它与生物制剂的放射性标记碎片结合,并测量分离复合物的放射性。这种方法的一个重要优点是,生物制剂处于溶液中,由于涂层而发生变性的可能性很低。此外,类风湿因子结合或非特异性抗体结合导致假阳性的风险较低。放射免疫分析法的缺点包括测试的复杂性,孵化时间长和使用的安全问题。
5.同时服用抗增殖和/或免疫抑制药物,如甲氨蝶呤,通过各种机制减少ADA的形成并维持血清药物浓度。
6.已提出定期监测血清药物和ADA水平,但尚未将其引入风湿病临床诊治实践,这主要是由于缺乏成本效益数据。

全部评论